Kovalens kötések vs. Ionos kötések
Tartalom
- Tartalom: Különbség a kovalens kötések és az ionos kötések között
- Összehasonlító táblázat
- Mi az a kovalens kötvény?
- Mi az ionos kötések?
- Főbb különbségek
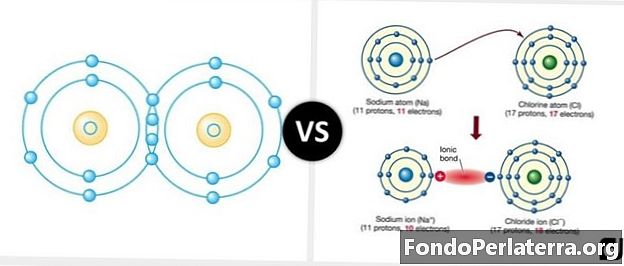
Az ionos és a kovalens kötés közötti különbség az elektronpárok és atomok megoszlása. Kovalens kötésekben az atomok elektrosztatikusan vonzódnak egymáshoz, míg ionos kötésekben; az elektronpárok megoszlanak az atomok között.

Tartalom: Különbség a kovalens kötések és az ionos kötések között
- Összehasonlító táblázat
- Mi az a kovalens kötvény?
- Mi az ionos kötések?
- Főbb különbségek
- Videó magyarázat
Összehasonlító táblázat
| A megkülönböztetés alapjai | Kovalens kötések | Ionos kötvények |
| Meghatározás | A kovalens kötés egyfajta kémiai kötés, amely magában foglalja megosztott párok vagy kötési párok (elektronpárok) megosztását az atomok között. | Az ionos kötés az a kémiai kötés, amely magában foglalja az egy vagy több elektron megosztását vagy teljes leadását az egyik atomból a másikba. |
| Esemény | A kovalens kötések a semleges atomok kölcsönhatásának eredményei | Az ionkötések az anionok és a kationok közötti kölcsönhatás eredményei. |
| Kémiai potenciál | Ezek meglehetősen gyenge kémiai kötések | Ez a kémiai kötés legerősebb típusa. |
| Képződés | A nemfémes elemek kovalens kötéseket képeznek | A fém elemek ionos kötéseket képeznek |
| Az elektronok állapota | Megosztott elektronok | Teljes elektronátvitel |
| Az ügy állapota | Folyadékok és gázok szobahőmérsékleten | Szilárd anyag szobahőmérsékleten |
| vegyületek | Organikus | Szervetlen |
| Oldhatóság | Vízben nem oldódik | Vízben oldódik |
| Alak | Határozott alak | Nincs határozott alak |
| elnevezési | Görög előtagok | római számok |
| Példák | Sósav és metán | Kénsav és nátrium-klorid |
Mi az a kovalens kötvény?
A kovalens kötés, amelyet molekuláris kötések néven is ismert, az a kémiai kötés, amely megosztott párok vagy kötési párok (elektronpárok) megosztását foglalja magában az atomok között. A legtöbb molekulában az elektronok megosztása lehetővé teszi, hogy minden atom teljes külső héjnak megfelelő egyenértékű anyagot kapjon, amely megfelel a stabil elektronikus konfigurációnak. Ha az atomok hasonló affinitással rendelkeznek az elektronokkal szemben, akkor valószínűleg kovalens kötések lépnek fel, mivel ugyanaz az affinitás az elektronokkal szemben, és nincs hajlandóság az atomok adományozására. Az atomok megosztják az elektronokat, hogy oktet-konfigurációt kapjanak, és stabilabbá és erősebbé váljanak. A szigma és a pi orbitál kölcsönhatása miatt a kovalens kötések négy típusú kötést képezhetnek, nevezetesen egy, kettős, hármas és négyszeres kötéseket. Az oxigénatomok a legjobb példa arra, hogy két további elektronra van szükség egy zárt héj kialakításához, míg a hidrogénatomoknak szükségük van egyre a zárt héj kialakításához. Az oxigénatom elektronjainak két része hidrogénatomokkal oszlik meg, tehát mindkét atomjának zárt héja van. Ez végül létrehoz egy vízmolekulát.
Mi az ionos kötések?
Az ionos kötés az a kémiai kötés, amely magában foglalja az egy vagy több elektron megosztását vagy teljes leadását az egyik atomból a másikba. Az ionkötések azoknak az elemeknek az eredménye, amelyek könnyen elveszítik az elektronokat, és azok az elemek, amelyek elektronokat nyernek. Az ilyen típusú kötések egyáltalán nem vonatkoznak a molekulákra a töltések közötti kölcsönhatás miatt, amint azt a Coulomb-törvény írja le. Az ionkötések szobahőmérsékleten szilárdak maradnak, mivel az egymilliárd ionokkal rendelkező periodikus rácsok során minden ion sok ellentétes töltésű ionnal van körülvéve. A negatív és a pozitív ionok közötti elektrosztatikus vonzások együtt tartják a vegyületet. Az ionos kötés során a teljes energia általában pozitív, jelezve, hogy a reakció endoterm és kedvezőtlen. Másrészt ez a reakció ugyanakkor kedvező az elektrosztatikus vonzerejük miatt. Az ionos kötés általános példája a nátrium vagy a só. A nátrium-atomok gyorsan elektronokat adnak, amelyek pozitív töltést eredményeznek. A klór elfogadja ezeket az elektronokat és negatív töltésű. Ez a két ellentétesen töltött atom ezután vonzza egymást, hogy nátrium-klorid molekulát képezzen.
Főbb különbségek
- A kovalens kötésekben az elektronpályák egymást átfedik, míg ionos kötések esetén ezek külön vannak.
- A kovalens kötések viszonylag lágyak az ionos kötésekhez képest, amelyek kemények és törékenyek.
- Mind a fém, mind a nem fém atomok részt vesznek az ionkötések kialakulásában, míg a kovalens kötések kialakulásában; csak nemfémek atomjai vannak jelen.
- Kovalens kötések az elektronok megosztása miatt képződnek, míg az ionos kötések az elektronok átvitele miatt lépnek fel.
- A molekulák a vegyületképződés során a kovalens kötésekben levő részecskék, míg az ionkötésekben ezek pozitív és negatív töltésű ionok.
- A kovalens kötések nem vezetnek, míg az ionos kötések vezetnek.
- Kovalens kötés történik az atomok között, amelyek elektronegativitása kevéssé különbözik. Ionos kötés történik az atomok között, amelyek nagy különbséget mutatnak az elektronegativitásban.
- Az ionkötések magas olvadást és forráspontot igényelnek ionos kötések esetén. A kovalens kötés alacsony olvadáspontú és forráspontot igényel kovalens kötés esetén.
- A metán és a sósav a kovalens nátrium-klorid és a kénsav általános példái az ionos kötések.
- A kovalens kötéseknek meghatározott alakjuk van, míg az ionos kötéseknek nincs határozottak
- A kovalens kötések alacsony polaritásúak, míg az ionos kötések magas polaritásúak.
- A 100% kovalens molekulák oldódnak az olajban, de nem a vízben, bár sok ionos kötés képes vízben oldódni, de az olajban nem.
- A kovalens kötések azért fontosak, mert a szénmolekulák elsősorban kovalens kötéssel lépnek kölcsönhatásba, míg az ionos kötések fontosak, mivel ezek lehetővé teszik bizonyos szerves vegyületek szintézisét.
- A kovalens kötések lehetnek elemek és vegyületek is, míg az ionos kötések csak vegyületek lehetnek.